
Ученые из Института общей и неорганической химии им. Н.С. Курнакова РАН, Национального медицинского исследовательского центра онкологии им. Н.Н. Блохина, Национального исследовательского университета «Высшая школа экономики» и Национального исследовательского ядерный университета «МИФИ» синтезировали новый перспективный агент для лечения рака методом бор-нейтронозахватной терапии. На основе конъюгатов клозо-додекаборатного аниона, выступающего в качестве источника бора и аминокислот, в качестве векторного фрагмента были получены вещества (производные), распознаваемые центрами связывания большой системы нейтральных транспортеров аминокислот, которая служит мишенью для клинически применяемых для данного типа терапии агентов. Разработка перспективна для более качественной радиотерапии. Работа выполнена при поддержке Российского научного фонда (№ 24-13-00295) и опубликована в журнале International Journal of Molecular Sciences.
Бор-нейтронозахватная терапия (БНЗТ) — активно развивающийся метод лечения сложных случаев рака. Этот метод основан на селективном разрушении опухолевых клеток при облучении тепловыми нейтронами. Ее эффективность во многом зависит от селективного накопления и удержания в опухолевых клетках лекарственных препаратов, содержащих нерадиоактивный изотоп бор-10, который выступает в роли мишени для нейтронов. Поиск новых потенциальных менее токсичных и более специфичных препаратов является одной из важнейших задач, для успешного внедрения данного вида терапии в широкую клиническую практику. Коллектив ученых из Москвы синтезировал новые соединения с потенциальным применением для разработки новых агентов для бор-нейтронозахватной терапии.
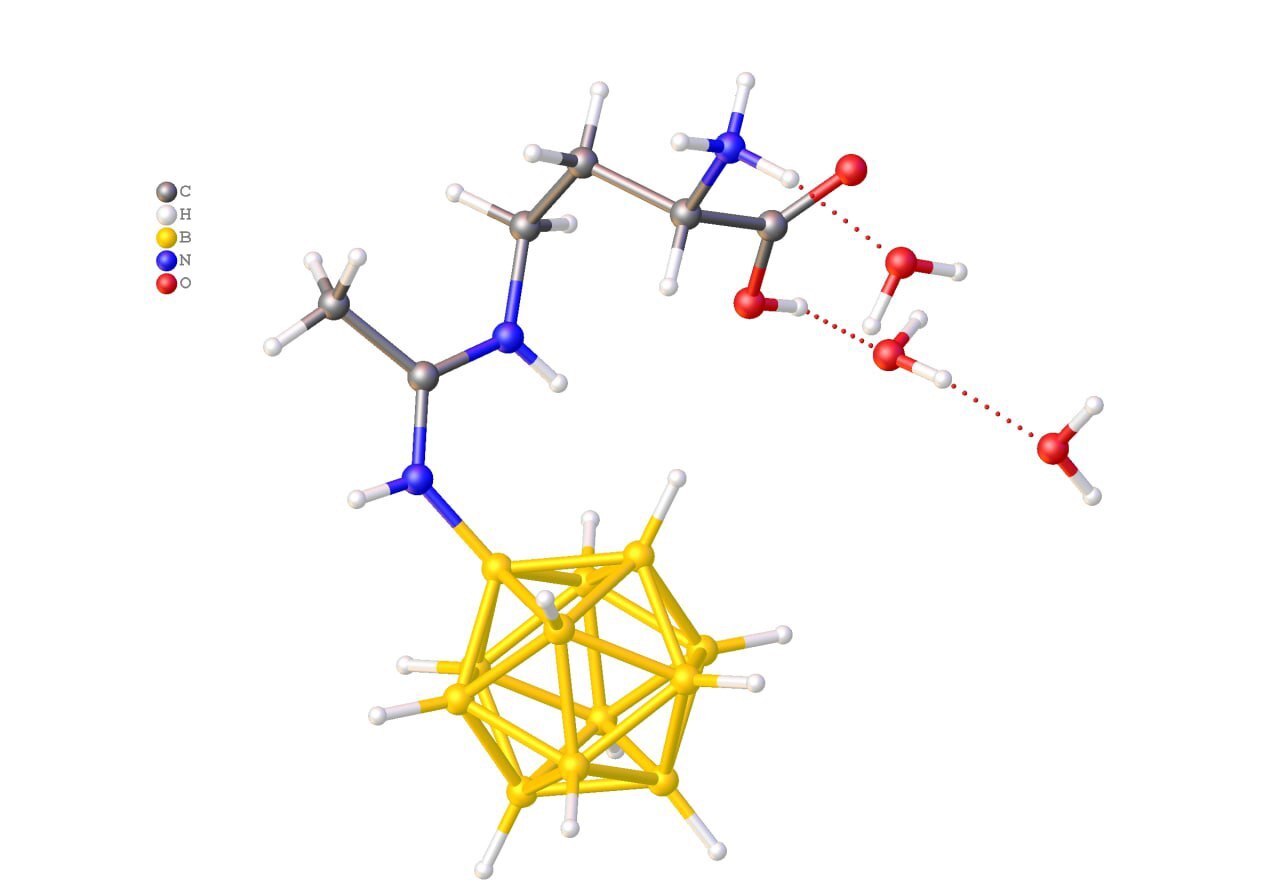
Исследование прокомментировал старший научный сотрудник Лаборатории химии легких элементов и кластеров ИОНХ РАН, кандидат химических наук Андрей Жданов: «Существует достаточно большое число способов модификации клозо-додекаборатного аниона, которые позволяют вводить в молекулу активную группу. В данном исследовании нами была использована стратегия синтеза на основе реакций активированных органических нитрилов и некоторых диаминокислот. Модификация протекает по аминогруппе, находящейся в боковой цепи. При этом фрагмент аминокислоты не затрагивается и успешно распознается центрами связывания белка-транспортера LAT1, что позволяет достичь селективности накопления соединения бора в опухолевых тканях.
Для всех синтезированных соединений авторы исследовали их острую токсичность и определили значения полулетальной дозы (LD 50). По результатам токсикологических исследований было выбрано одно соединение для исследования поглощения in vivo на двух моделях опухолей. Выбранное соединение показало низкую токсичность (LD 50 в диапазоне от 150 до 300 мг/кг) и отличную растворимость, а также избирательное поглощение при экспериментальной меланоме у лабораторных животных».
В работе предложено несколько подходов к синтезу целевых соединений, и оптимизированы условия проведения реакций для масштабирования процесса их получения. По словам авторов, созданный новый аналог (новое соединение) соединения бора поможет оптимизировать бор-нейтронозахватную терапию. В дальнейшем авторы планируют расширить спектр транспортных функциональных групп, а также работать над повышением эффективности и селективности накопления таких конъюгатов, в том числе за счет выбора и оптимизации лекарственных форм.