
Ученые оценили, как меняются токсичность и антиоксидантные свойства наночастиц оксида железа в зависимости от температуры, при которой их отжигают после синтеза радиационно-химическим способом. В результате авторам удалось получить наночастицы, которые подавляют рост раковых, но не здоровых клеток, а также эффективно борются с окислительными процессами, приводящими к повреждению мембран и ДНК. Благодаря этому наночастицы потенциально могут использоваться в составе противоопухолевых препаратов. Результаты исследования, поддержанного грантом Российского научного фонда (РНФ), опубликованы в журнале Ceramics International.
Наночастицы оксида железа перспективны для использования в медицине и фармацевтике. Так, на их основе разрабатывают системы доставки лекарств, перемещением которых можно управлять с помощью магнита. Кроме того, такие наночастицы подавляют рост болезнетворных бактерий, в том числе устойчивых к антибиотикам.
Ученые из Института электрофизики Уральского отделения РАН (Екатеринбург) ранее предложили получать наночастицы оксида железа радиационно-химическим методом. Он заключается в том, что раствор с железосодержащими веществами-предшественниками облучают пучком электронов, под действием которых образуется нерастворимый оксид железа. Затем наночастицы дополнительно обрабатывают при высоких температурах — отжигают. При этом их физические свойства (размер, текстура, способность намагничиваться) оказываются разными в зависимости от поглощенной дозы электронного пучка, температуры отжига и вещества-предшественника. Однако как условия синтеза влияют на характеристики частиц, особенно важные в медицине, — в частности, токсичность и способность бороться с окислением (антиоксидантные свойства), — оставалось не до конца понятным.
В новой работе авторы с коллегами из Уральского федерального университета (Екатеринбург) и Института иммунологии и физиологии Уральского отделения РАН (Екатеринбург) синтезировали радиационно-химическим методом наночастицы оксида железа из двух соединений-предшественников — нитрата и сульфата железа. Затем их отжигали при разных температурах — от 100 до 1050°C.
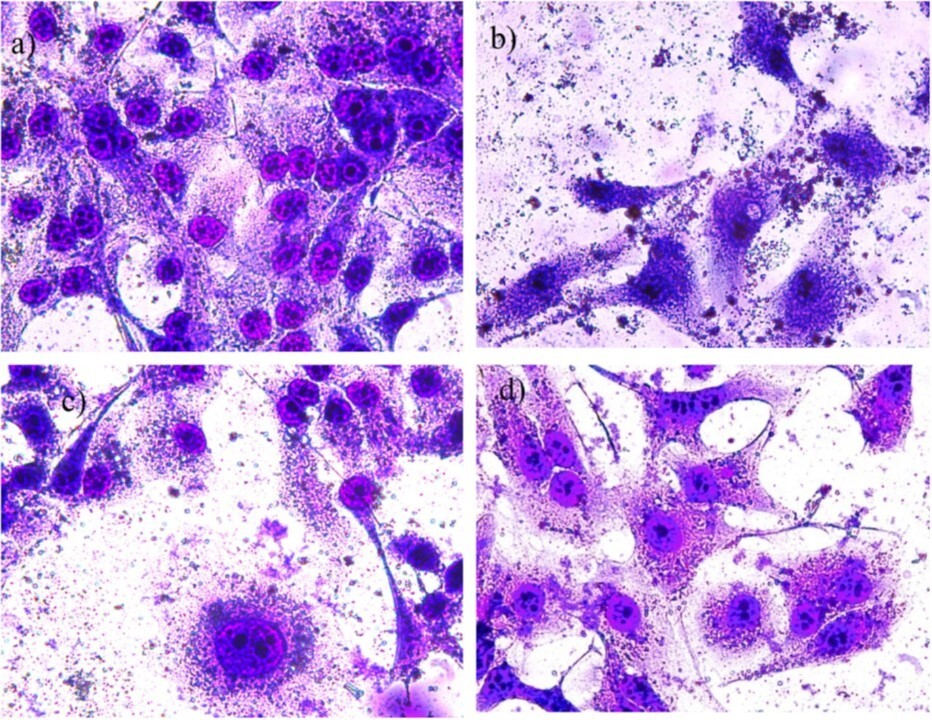
Исследователи проверили действие наночастиц в разной концентрации (от 0,1 до 1 миллиграмма на литр раствора) на клетках рака шейки матки и фибробластах — клетках соединительной ткани. Оказалось, что наночастицы, синтезированные из сульфата железа и обработанные при температуре 400°C, приводят к гибели 94% клеток рака шейки матки. При этом в отношении фибробластов такого губительного эффекта не наблюдалось — жизнеспособность этой культуры уменьшилась всего на 12–28% в зависимости от количества нанесенных на клетки частиц.
Наименее токсичными в отношении обоих исследованных типов клеток оказались наночастицы, которые отжигали при 300°C: в самой низкой концентрации они практически не снижали жизнеспособность клеток, а в самой высокой — уменьшали ее на 29%.
Чтобы проверить антиоксидантные свойства наночастиц, авторы искусственно смоделировали в культурах клеток окислительный стресс, добавив к ним перекись водорода. Эта молекула вырабатывается при избыточном окислении и повреждает мембраны, ДНК и другие клеточные структуры. Эксперименты показали, что наночастицы, полученные из сульфата железа и обработанные при 400°C, лучше всего защищают клетки от окислительных процессов, уменьшая количество перекиси на 65%. Благодаря тому, что такие наночастицы сочетают в себе антиоксидантную активность, высокую токсичность в отношении раковых клеток и при этом низкую в отношении здоровых, они могут использоваться для разработки новых противоопухолевых препаратов.
«В дальнейшем мы планируем продолжить исследования физико-химических и биологических свойств наночастиц оксидов железа, в том числе покрытых нанослоем серебра», — рассказывает руководитель проекта, поддержанного грантом РНФ, Сергей Соковнин, доктор технических наук, ведущий научный сотрудник группы электрофизических технологий Института электрофизики Уральского отделения РАН.