Ученые выяснили, как внеклеточные структуры влияют на рост метастазов раковых опухолей
Зависимость между биомеханическими свойствами внеклеточного матрикса и развитием опухолевых клеток в нем доказали ученые Института регенеративной медицины, Института молекулярной тераностики и Лаборатории клинических смарт-нанотехнологий Сеченовского Университета Минздрава России. Это позволит создавать более реалистичные модели для изучения роста раковых опухолей и метастазов, что даст возможность лучше понимать особенности развития разных форм рака в тех или иных органах и их метастазирования, и, соответственно, точнее прогнозировать развитие болезни и подбирать терапию. Работа велась совместно с ИБХ РАН и ННГУ им. Лобачевского. Статья опубликована в журнале Cells.
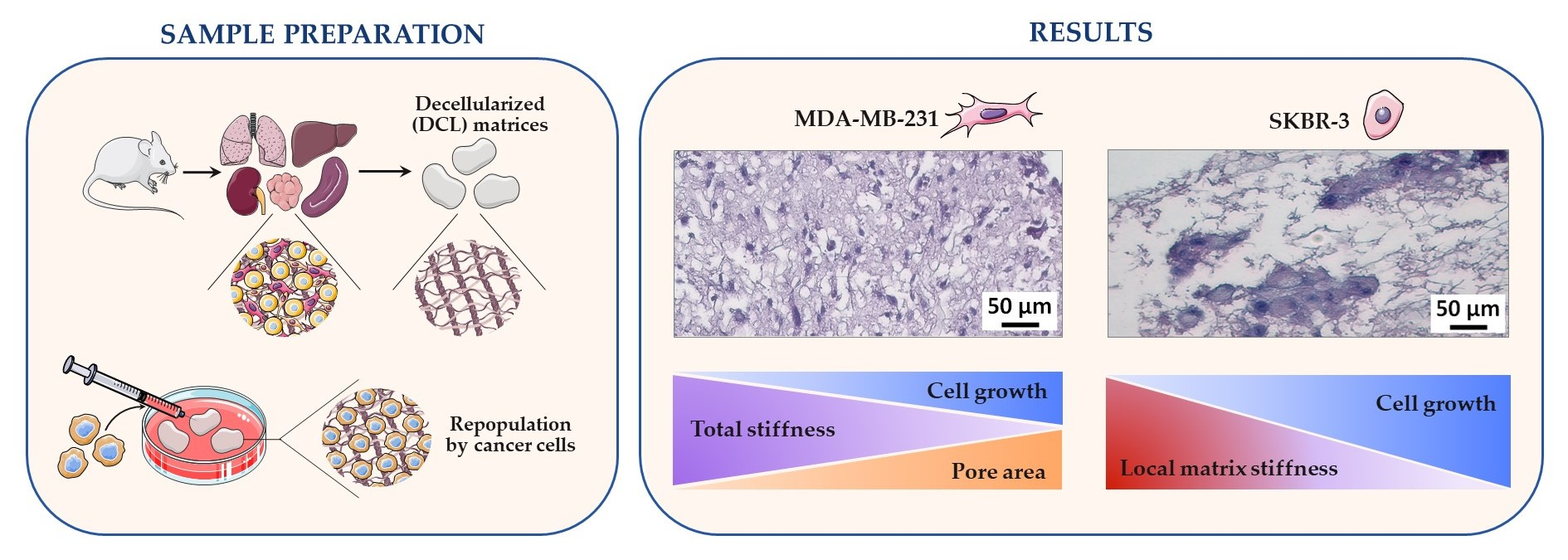
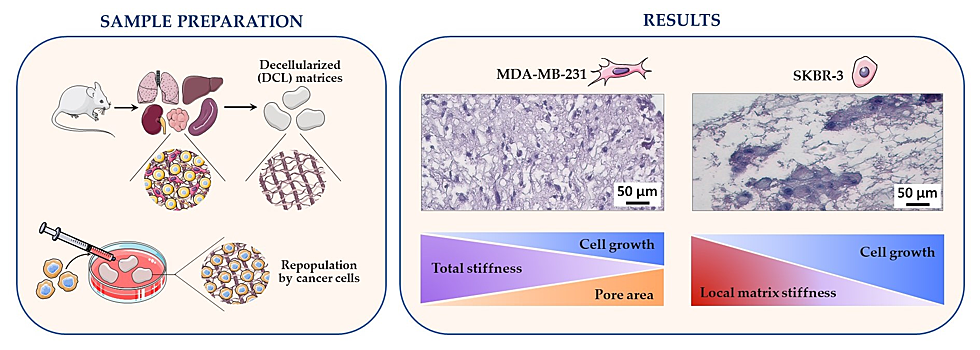
Децеллюляризация — это процедура очистки тканей или целых органов от клеточного компонента. С ее помощью можно получить конструкцию на основе естественного внеклеточного матрикса — структуры, играющей роль "каркаса", который обеспечивает механическую поддержку клеток. Изменения состава и свойств внеклеточного матрикса тесно связаны с развитием опухолей, поэтому использование конструкций на его основе играет важную роль в изучении механизмов образования опухолей и поиске средств от рака.
Существующие сегодня методы децеллюляризации годятся лишь для нескольких органов, что ограничивает ученых в выборе материалов для исследования. Поэтому специалисты разработали собственный протокол децеллюляризации, подобрав для этого среды, не нарушающие целостность волокон матрикса и подходящие для очистки разных тканей. Раковые опухоли способны метастазировать в разные органы, поэтому важно иметь возможность работать с наибольшим их количеством.
Ученые использовали печень, легкие, селезенку, почки и яичники 30 мышей. Очистив органы от клеток, исследователи измерили основные биомеханические параметры матрикса: жесткость, размер пор и диаметр белковых волокон. Они установили, что структура матрикса тканеспецифична: так, матрикс легких имеет наименьшую жесткость и наибольший размер пор, а матрикс почек, напротив, представляет из себя структуру с наибольшей жесткостью и наименьшим размером пор.
Чтобы выяснить, как эти параметры влияют на рост и развитие опухолевых клеток, ученые заселили матриксы клетками разных линий рака молочной железы: MDA-MB-231 и SKBR-3. По своей природе эти линии клеток сильно различаются. MDA-MB-231 — представитель трижды отрицательного рака молочной железы, низкодифференцированного и очень агрессивного. А линия SKBR-3, напротив, очень сильно походит на нормальные клетки и обладает низкой скоростью роста.
Как оказалось, клетки линии MDA-MB-231 предпочитают расти в матриксах с низкой общей жесткостью и большим размером пор, а клетки линии SKBR-3 лучше растут в матриксах с более низкой локальной жесткостью, при этом размер пор, по всей видимости, не играет особой роли. Таким образом, можно предположить, что в случае инвазивных клеток большой размер пор матрикса имеет решающее значение, поскольку он не препятствует миграции клеток, а для неинвазивных линий важна степень локальной жесткости, поскольку им нужно распространяться между волокнами матрикса.
"Механизмы метастазирования не изучены до конца, и ранее считалось, что основную роль в развитии метастазов играют химические факторы. Однако теперь есть веские основания полагать, что архитектура матрикса и биомеханика тоже вносят важный вклад", — отметил заместитель директора Института молекулярной тераностики Андрей Звягин.
Новые данные, в частности, позволят сделать более точными исследования предметастатических ниш — сред во вторичном органе, которые могут способствовать метастазированию первичной опухоли.
Материал подготовлен при финансовой поддержке Минобрнауки России в рамках федерального проекта «Популяризация науки и технологий».